# SARS-CoV-2, COVID-19, слюна, комплект диагностики
Аннотация
быстрый и точный SARS-CoV-2 диагностическое тестирование имеет важное значение для контроля над продолжающейся COVID-19 пандемия. Текущий золотой стандарт для COVID-19 диагностика в режиме реального времени ОТ-ПЦР обнаружение SARS-CoV-2 из мазки из носоглотки. низкая чувствительность, риски воздействия на медицинских работников и глобальная нехватка тампонов и средств индивидуальной защиты, однако, требуют проверки новых диагностических подходов. слюна - многообещающий кандидат на SARS-CoV-2 диагностика потому что (1) сбор является минимально инвазивным и может быть самостоятельным и (2) слюна показала сопоставимую чувствительность к мазкам из носоглотки при обнаружении других респираторных патогенов, включая эндемичные коронавирусы человека, в предыдущих исследованиях. К подтвердить использование слюны для SARS-CoV-2 обнаружения, мы проверили образцы носоглотки и слюны из подтверждено COVID-19 пациентов и самостоятельно собранные образцы из медицинские работники COVID-19 подопечные. Когда мы сравнили SARS-CoV-2 обнаружение от подобранный к пациенту носоглоточный
и образцы слюны, мы обнаружили, что слюна дает большую чувствительность обнаружения и последовательность на протяжении всего периода заражения. Кроме того, мы сообщаем о меньшей изменчивости собственной выборки сбор слюны. взятые вместе, наши результаты демонстрируют, что слюна является жизнеспособной и более чувствительной альтернативой мазкам из носоглотки и включить дома самоуправляемый сбор образцов для точного крупномасштабного SARS-CoV-2 тестирование.
введение
усилия по борьбе с SARS-CoV-2, новым коронавирусом вызывающий COVID-19 пандемии, зависят от точной и быстрой диагностики тестирования. Эти тесты должны быть ( 1 ) чувствительны к легким и бессимптомным инфекциям, что способствует эффективной самоизоляции и сокращению передачи в группах высокого риска1 ; ( 2 ) согласован для надежного мониторинга прогрессирования заболевания и оказания помощи в принятии клинических решений2 ; и ( 3 ) масштабируемость для информирования местных и национальных политик общественного здравоохранения, таких как когда меры социального дистанцирования можно безопасно смягчить. Однако текущая SARS-CoV-2 стратегии тестирования часто не соответствуют этим критерии, отчасти потому, что их использование мазков из носоглотки как широко рекомендуемого типа образцов для ОТ-ПЦР в реальном времени.
Хотя мазки из носоглотки широко используются в диагностике респираторных вирусов, они показывают относительно низкую чувствительность к SARS-CoV-2 выявления на ранних стадиях инфицирования и составляют 2–6 непоследовательно во время серийное тестирование . Кроме того, забор мазков из носоглотки вызывает дискомфорт у пациентов из-за инвазивность, ограничивающая возможность повторного тестирования, и представляет значительный риск для медицинских работников, потому что он может побуждать пациентов чихать или кашлять, выводя вирус частицы7 , Процедура также не способствует масштабному тестированию, потому что повсеместно ощущается нехватка тампонов и средств индивидуальной защиты для медицинских работников8 , и самовывоз мазков из носоглотки сложен и менее чувствителен к вирусам обнаружение9 , Эти проблемы будут усугубляться по мере того, как COVID-19 пандемия усиливается в странах с низким доходом. с учетом ограничений, более надежный и менее ресурсоемкий метод сбора образцов, в идеале такой, который позволяет самостоятельно собирать в доме, необходимо срочно. забор слюны является привлекательной альтернативой мазку из носоглотки, поскольку сбор слюны неинвазивный и проста в самоуправлении. анализ конкордантности носоглотки и слюны для ОТ-ПЦР обнаружение респираторных возбудителей, в том числе двух сезонных
человеческие коронавирусы, предполагает сравнимую диагностическую чувствительность двух образцов 10,11 COVID-19 пациенты и ( 2 ) Самостоятельно собранные образцы слюны сопоставимы. предварительные данные показывают, что ( 1 ) SARS-CoV-2 можно обнаружить из слюна 12 typesmSARS-CoV-2 чувствительность обнаружения к мазкам из носоглотки, собранным медицинскими учреждениями 13 рабочие из легкая и субклиническая форма COVID-19 случаи . Однако крайне важно отсутствие строгой оценки чувствительности SARS-CoV-2 обнаружение в слюне в отношении мазков из носоглотки стационарные во время течение COVID-19 инфекции.
в этом исследовании мы оценили SARS-CoV-2 обнаружение в парных мазках из носоглотки и образцах слюны, взятых из COVID-19 стационарных больных и бессимптомных медицинских работников в средней и высокой риск COVID-19 экспозиции. Наши результаты показывают, что использование слюны для SARS-CoV-2 обнаружение более чувствительно и последовательно, чем с помощью назофарингеальных мазков. В целом, мы демонстрируем, что слюна должна считаться надежным типом образцов для облегчения COVID-19 тестирование требований.
полученные результаты
высшее SARS-CoV-2 обнаружены титры от слюна чем мазки из носоглотки стационарные пациенты
К определить, работает ли слюна так же хорошо, как и США. Рекомендация cdc по использованию мазков из носоглотки при SARS-CoV-2 диагностики, мы собрали клинические образцы из 44 COVID-19 участники стационарного исследования ( Таблица 1 ). Это когорта представляет собой диапазон COVID-19 пациентов с тяжелым заболеванием, с 19 (43%) нуждающиеся в интенсивной терапии, 10 (23%) требующие искусственной вентиляции легких, и 2 (5%) скончался 5 апреля 2020 г. используя США cdc SARS-CoV-2 ОТ-ПЦР 121 самостоятельный сбор слюны или медицинское обслуживание мазки из носоглотки эта когорта. Мы обнаружили сильное согласие между США. cdc «N1» и «N2» праймер-зонд наборы ( расширенные данные Рис. 1), и таким образом рассчитанные титры вируса (вирус копий / мл) используя только «N1» набор. От все положительные образцы протестированы ( п = 46 носоглотки, 37 слюны), мы обнаружили, что средние геометрические титры вируса от слюны были около 5⨉ выше чем мазки из носоглотки ( п < 0,05, Манн-Уитни тест; Рис. 1a ). Когда ограничивая наш анализ только подобранным пациентом образцы носоглотки и слюны ( п = 38 для каждого типа образцов), мы обнаружили, что SARS-CoV-2 титры от слюны были значительно выше чем мазки из носоглотки ( п = 0,0001, Вилкоксон тест; Рис. 1b ). Кроме того, мы обнаружили SARS-CoV-2 из слюна, но не мазки из носоглотки из восемь совпадающих образцов (21%), в то время как мы обнаружили только SARS-CoV-2 из мазки из носоглотки, а не слюна три согласованных образца (8%; Рис. 1c ). В целом мы обнаружили, что SARS-CoV-2 титры от слюна чем мазки из носоглотки больница стационары.
стол 1. COVID-19 характеристики когорты стационарных пациентов
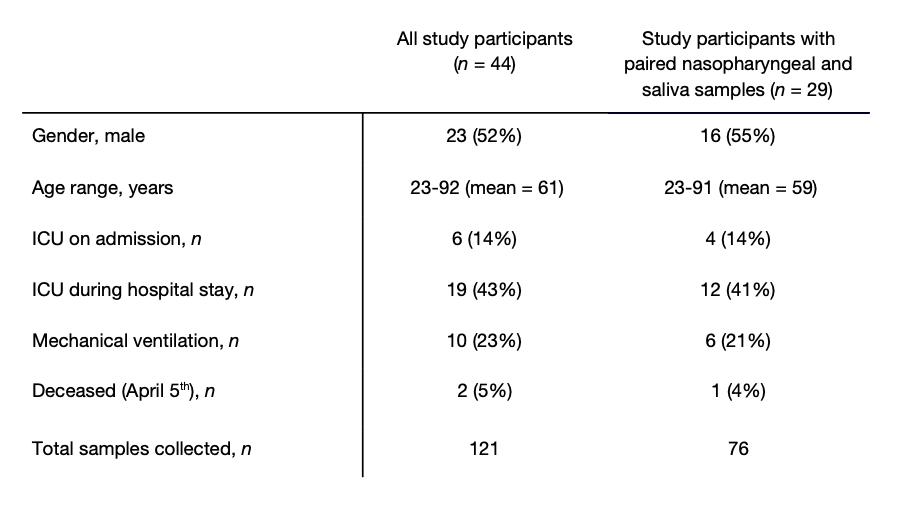
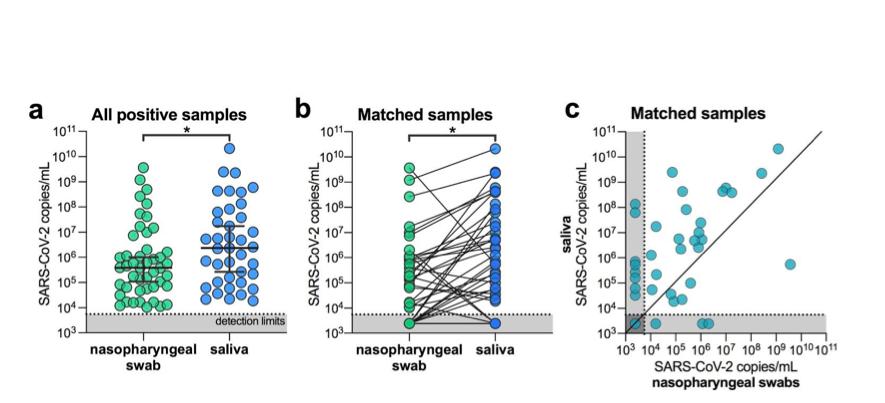
рисунок 1. SARS-CoV-2 титры в слюне выше, чем мазки из носоглотки больница стационары. ( а ) все положительные мазки из носоглотки ( п = 46) и образцы слюны ( п = 39) сравнивались с помощью Манна-Уитни тест ( п < 0,05). столбцы представляют собой медианное значение и 95% CI. Наши пределы обнаружения для SARS-CoV-2 используя американский CDC «N1» анализ находится на пороге цикла 38, что соответствует 5610 копий / мл вируса образца (показаны пунктирной линией и серой областью). ( б ) образцы, соответствующие пациенту ( п = 38), представленные соединительными линиями, сравнивались с помощью Вилкоксона тестовый тест ( п < 0,05). ( c ) образцы, соответствующие пациенту ( п = 38) также представлены на диаграмме рассеяния. все данные, использованные для генерации этой цифры, включая необработанные пороги цикла, можно найти в дополнительные данные 1 , расширенные данные Рис. 1 показывает корреляцию между нами cdc assay «N1» и «N2» результаты.
менее временный SARS-CoV-2 изменчивость когда тестирование слюны от стационарные пациенты
как временный SARS-CoV-2 диагностическое тестирование от мазки из носоглотки 2,3переменной, мы протестировали продольные образцы носоглотки и слюны из стационарных больных, чтобы определить, какой тип образца дает более согласованные результаты. От 22 участника с несколькими мазками из носоглотки и 12 участников с несколькими образцами слюны, мы обнаружили, что SARS-CoV-2 титры обычно снижались в обоих типах образцов после указанной даты появления симптомов ( Рис. 2а ). Наши результаты мазка из носоглотки соответствуют 2,3предыдущие отчеты о переменной SARS-CoV-2 титры и результаты : мы нашли 5 экземпляров где участника мазок из носоглотки оказался отрицательным на SARS-CoV-2 с последующим положительным результатом во время следующий сбор (5 / 33 повторов, 33%; Рис. 2b ) , в продольных сборах слюны от У 12 пациентов, однако, не было случаев, когда образец давал отрицательный результат, а затем давал положительный результат. поскольку истинно отрицательные результаты тестов важны для клиницистов для отслеживания улучшений состояния пациентов и для принятия решений относительно выписки, наши данные показывают, что слюна является более последовательным типом образца, чем мазки из носоглотки для мониторинга временных изменений SARS-CoV-2 титров.
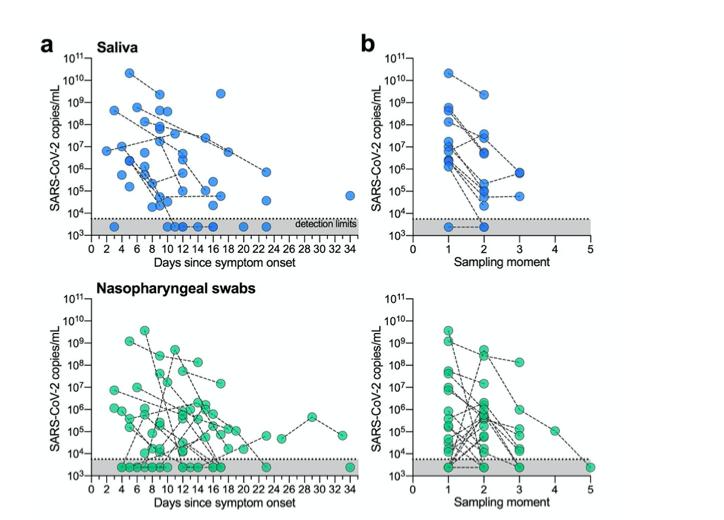
рисунок 2: SARS-CoV-2 обнаружение менее вариабельно между повторными сборами образцов с слюной. (а) продольный SARS-CoV-2 титры от слюна или мазки из носоглотки показаны как дни с симптом начало. каждый кружок представляет собой отдельный образец, к которому подключены дополнительные образцы из того же пациента пунктирной линией. Наши пределы обнаружения для SARS-CoV-2 используя американский CDC «N1» анализ находится на пороге цикла 38, что соответствует 5610 копий / мл вируса образца (показаны пунктирной линией и серой областью). ( б ) Данные также отображаются по моменту выборки (последовательный сбор время) , чтобы подчеркнуть различия в титрах вирусов между точками сбора все данные, использованные для генерации этой цифры, включая необработанные пороги цикла, можно найти в дополнительные данные 1 ,
более последовательная самовыборка из медицинские работники, использующие слюну
проверка слюны для выявления субклинического SARS-CoV-2 инфекции могли доказать преобразующий как для удаленной диагностики пациентов, так и для медицинских работников наблюдения. К расследуя это, мы набрали 98 бессимптомных медицинских работников в наше исследование и собранная слюна и / или мазки из носоглотки в среднем каждые 2,9 дней (диапазон = 1-8 дней, Таблица 2 ). К дату, когда мы обнаружили SARS-CoV-2 в слюне из два медицинских работника, которые дали отрицательный результат мазка из носоглотки с использованием обоих американских CDC «N1» и «N2» тесты и не сообщали о каких-либо симптомах. Слюна от один из этих люди снова дали положительный результат вместе с соответствующим отрицательным мазком из носоглотки повторное тестирование через 2 дня. титры вирусов от бессимптомное лечение рабочих слюны ниже, чем что мы обычно обнаруживаем из симптоматические стационарные больные ( Рис. 3a ), что, вероятно, свидетельствует об отсутствии симптомов.
Наши ограниченные данные подтверждают, что слюна может быть более чувствительной для выявления бессимптомных или предсимптомных инфекции; однако для подтверждения требуется больший размер выборки. поскольку несоответствие образцов мазка из носоглотки может быть одной из потенциальных проблем для ложноотрицательных результатов ( Рис. 2), мониторинг внутреннего контроля для надлежащего сбора образцов, человеческой РНКазы P, может предоставить альтернативный метод оценки. в то время как обнаружение человеческой РНКазы p было лучше из слюна в когортах как стационарных пациентов, так и медицинских работников ( Рис. 3b ) , само по себе это не может указывать на лучшее обнаружение вирусов. что более важно, мы обнаружили, что определение человеческой РНКазы p было более вариабельным из мазки из носоглотки собраны из стационарные ( п = 0,0001, f тест на дисперсии) и самовывозом из работники здравоохранения ( п = 0,0002; Рис. 3b ). Наши результаты показывают, что слюна также может быть подходящей и, возможно, более чувствительной альтернативой мазкам из носоглотки для выявления бессимптомных или предсимптомных SARS-CoV-2 инфекции.
стол 2. когорта медицинских работников
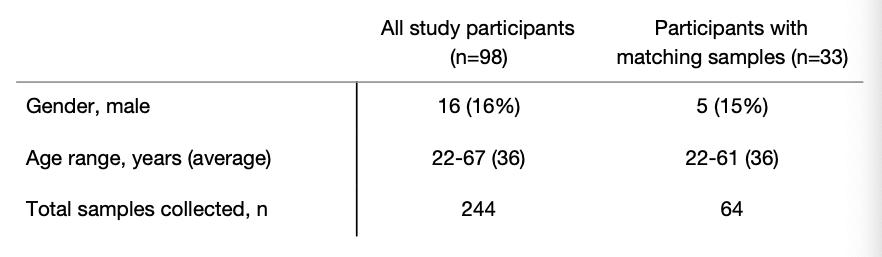
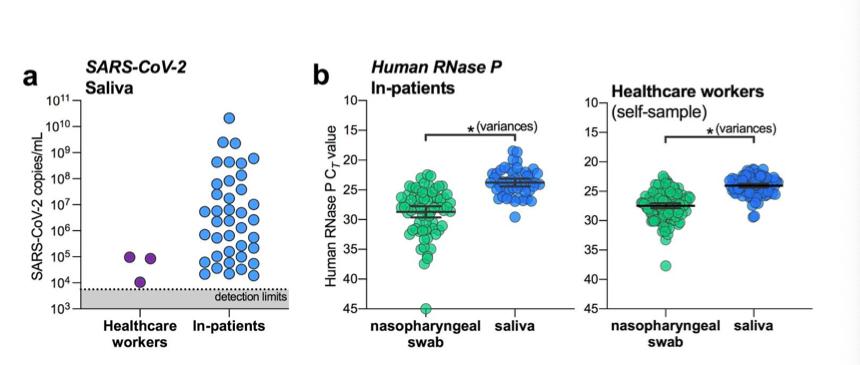
рисунок 3. слюна - альтернатива SARS-CoV-2 экранирование от медицинские работники и бессимптомные случаи. ( а ) SARS-CoV-2 титры измерены от слюна медицинских работников и стационарных больных. Наши пределы обнаружения для SARS-CoV-2 используя американский CDC «N1» анализ находится на пороге цикла 38, что соответствует 5610 копий / мл вируса образца (показаны пунктирной линией и серой областью). ( б ) ОТ-ПЦР пороги цикла (Ct) значения для человеческой РНКазы P и внутреннего контроля для сбора образцов, от либо стационарные (левая панель) или медицинские работники (правая панель) сравнивались по дисперсиям с использованием критерия f ( п = 0,0001 для стационарных больных; п = 0,0002 для здравоохранения работников). все данные, использованные для генерации этой цифры, включая необработанные пороги цикла, можно найти в дополнительные данные 1 ,
обсуждение
Наши исследование показывает, что слюна является жизнеспособной и предпочтительной альтернативой мазкам из носоглотки при SARS-CoV-2 обнаружения. Мы установлено, что чувствительность SARS-CoV-2 обнаружение от слюна сопоставима, если не превосходит мазки из носоглотки при ранней госпитализации и более стабильна во время длительная госпитализация и выздоровление. Более того, обнаружение SARS-CoV-2 из слюна двух бессимптомных медицинских работников, несмотря на отрицательные результаты мазков из носоглотки, предполагает, что слюна также может быть жизнеспособной альтернативой для выявления легких или субклинических инфекций. С дальнейшая проверка, широкое внедрение забор слюны мог быть преобразующим для общественного здравоохранения усилия: слюна самовывоз устраняет необходимость в непосредственной медицинской помощи работник-пациент взаимодействие, источник 14–16 несколько основных узких мест при тестировании и общий риск внутрибольничных инфекций, а также снижает спрос на тампоны и средства индивидуальной защиты.
Вирусные нагрузки AsSARS-CoV-2 различаются между легкой и тяжелой формами , ограничение нашего исследования - основное внимание уделяется COVID-19 стационарных больных, многие с тяжелыми заболеваниями. в то время как требуется больше данных для более тщательного сравнения эффективности слюны в условиях больницы с более ранним течением инфекции, результаты два недавних исследования подтверждают его потенциал для 13,18 обнаружение SARS-CoV-2 из как бессимптомные, так и амбулаторные пациенты . в виде 12 инфекционный вирус обнаружен от слюна COVID-19 пациентов, выясняя связь между копиями вирусного генома и инфекционными вирусными частицами в слюне 19 предсимптоматический люди будут играть ключевую роль в понимании динамики 1,20 бессимптомная передача.
вытекающий из многообещающие результаты для SARS-CoV-2 обнаружение бессимптомного 13
отдельных лиц, как слюна Анализ SARS-CoV-2 уже получил одобрение в течение 18 лет.
нас. разрешение на использование пищевых продуктов и медикаментов в чрезвычайных ситуациях , К удовлетворяют растущие требования к тестированию, однако наши результаты подтверждают необходимость немедленной проверки и внедрения слюны на SARS-CoV-2 диагностика в сертифицированных клинических лабораториях.
методы
этика
все участники исследования были отобраны и отобраны в соответствии с требованиями Йельского университета Одобрено HIC протокол # 2000027690. Демографические, клинические данные и образцы были собраны только после того, как участник исследования признал, что они понял протокол исследования и подписал информированное согласие. вся информация об участниках и образцы были собраны вместе с идентификаторами исследования.
набор участников
стационарные пациенты
Медицинский центр третичной помощи на 1541 коек в Нью-Хейвене, штат Коннектикут, США, поступил в больницу Йельского Нью-Хейвена, у которых положительный результат теста на SARS-CoV-2 через носоглотку и / или мазок из ротоглотки (CDC одобрен анализ) были приглашены для участия в исследовании исследования. критериями исключения были возраст до 18 лет, неанглоязычный разговорные и клинические, радиологические или лабораторные доказательства неинфекционного причиной лихорадки или респираторных симптомов или микробиологически подтвержденного источник инфекции (например, желудочно-кишечный тракт, мочевой, сердечно-сосудистый) кроме дыхательных путей на наличие симптомов и отсутствие подозрений на COVID-19 инфекции.
работники здравоохранения
бессимптомные медицинские работники (например, без лихорадки или респираторных симптомов) с профессиональным воздействием на пациентов с COVID-19 были приглашены для участия в исследовании. участие в исследовании позволило провести активный надзор для обеспечения раннего обнаружения после заражения и для дальнейшей защиты других медицинских работников и пациентов.
сбор образцов
стационарные пациенты
образцы носоглотки и слюны брали каждые три дня на протяжении клинический курс. образцы носоглотки были взяты дипломированными медсестрами с использованием универсального вирусного транспорта bd (UVT) система. Гибкий, мини-наконечник мазок прошел через пациента ноздря пока была достигнута задняя часть носоглотки, оставлена на несколько секунд для впитывания секрета, а затем медленно удалена при вращении. Мазок помещали в стерильную среду для транспортировки вирусов (общий объем 3 мл) и запечатаны надежно. образцы слюны были взяты пациентом самостоятельно. По проснувшись, пациентов просили избегать еды, воды и чистки зубов до образец был собран. пациентов просили несколько раз плюнуть в стерильная чашка для мочи пока примерно на треть заполнена жидкостью (без пузырьков), прежде чем надежно закрыть все образцы хранились при комнатной температуре и транспортировались в исследовательскую лабораторию Йельской школы общественного здравоохранения в течение 5 часов после сбора образцов.
работники здравоохранения
медицинских работников попросили собрать самоуправления мазок из носоглотки и образец слюны каждые три дня в течение 2 недель. образцы хранились при + 4 ° C до транспортируется в исследовательскую лабораторию.
SARS-CoV-2 обнаружение
по прибытии в исследовательскую лабораторию, общее нуклеиновое кислота была извлечена из 300 мкл вирусных транспортных сред от мазок из носоглотки или 300 мкл цельной слюны с помощью MagMAX Вирусного / возбудителя Нуклеиновая набор для изоляции кислоты (ThermoFisher Scientific) после производителя протоколом и элюируется в 75 мкл буфера элюирования. Для SARS-CoV-2 rna 21,22 детектирование, 5 мкл шаблона РНК тестировали, как описано ранее, с использованием американского CDC в режиме реального времени RT-PCR праймер / зонд наборы для 2019-nCoV_N1 и 2019-nCoV_N2 и человеческая РНКаза p (RP) как добыча контроль. образцы были классифицированы как положительные на SARS-CoV-2 когда оба N1 и N2 праймер-зонд обнаружены наборы <38 c . копии вирусов были т количественно с использованием 10-кратного стандартная кривая разведения транскриптов РНК, которую мы ранее 21 годсгенерировано . как результаты из N1 и N2 были сопоставимы ( расширенные данные Рис. 1 ) все копии вирусов показаны рассчитанными с использованием N1 праймер-зонд набор.
статистический анализ
статистический анализ проводился в GraphPad призма 8.0.0 как описано в Результаты.
благодарности
Мы выражаем благодарность участникам исследования за их времени и приверженности к учебе. Мы поблагодарить всех членов клинической команды Yale-New больница-убежище для своих самоотверженность и работа, которые сделали это исследование возможным. Мы также благодарим S. Тейлор и П. домкрат для технических обсуждений.
финансирование
Исследование было частично профинансировано Йельским институтом глобального Здравоохранения. Авторы-корреспонденты имели полный доступ ко всем данным в исследовании и несли окончательную ответственность за решение о представлении для публикации.
расширенные данные
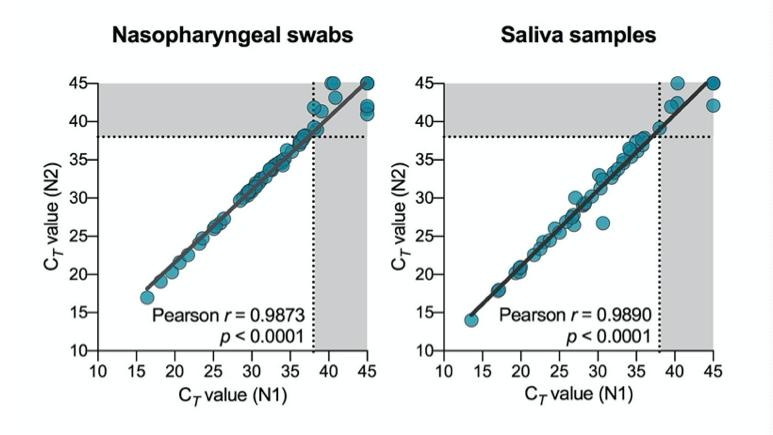
расширенные данные Рис. 1. соответствие между SARS-CoV-2 обнаружение с использованием us cdc «N1» и «N2» праймер и зонд наборы. ct = ОТ-ПЦР цикл порог. пунктирная линия и серые области обозначают пределы обнаружения.
Рекомендации
1. Кимбалл, А. et al. бессимптомный и бессимптомный SARS-CoV-2 инфекции у пациентов учреждения длительного ухода - округ Кинг, Вашингтон, март 2020 г. MMWR Морб. Смертный. Нед. Представитель 69, 377–381 (2020).
2. Вельфель, Р. et al. вирусологическая оценка госпитализированных пациентов с COVID-2019. природа (2020) DOI: 10.1038 / s41586-020-2196-x.
3. Цзоу, Л. et al. SARS-CoV-2 вирусная нагрузка в образцах верхних дыхательных путей инфицированных Пациенты. Н. Англ. J. Мед. 382 , 1177–1179 (2020).
4. Чжао, Дж. et al. ответы антител на SARS-CoV-2 у пациентов с новым коронавирусом болезнь 2019. Клин. Заразить. Дис. (2020) doi: 10.1093 / cid / ciaa344.
5. Се, X. et al. КТ грудной клетки для типичного 2019-нКоВ Пневмония: отношение к отрицательному ОТ-ПЦР Тестирование. радиология 200343 (2020).
6. Ван, W. et al. обнаружение SARS-CoV-2 в разных видах клинических образцов. JAMA (2020) DOI: 10.1001 / jama.2020.3786.
7. К, К. К.-В. et al. временные профили вирусной нагрузки в образцах задней ротоглотки слюны и сывороточные ответы антител во время заражение SARS-CoV-2: наблюдательное когортное исследование.ланцет Заражение. Дис. (2020) DOI: 10.1016 / S1473-3099 (20) 30196-1.
8. CDC. временные рекомендации по профилактике и контролю инфекций для пациентов с подозрением на коронавирус или подтвержденным болезнь 2019 (COVID-19) в здравоохранении Настройки. Центры по контролю и профилактике заболеваний https: / / www.cdc.gov / коронавирус / 2019-ncov / hcp / Инфекционный контроль-рекомендации.h tml? CDC_AA_refVal = https% 3A% 2F% 2Fwww.cdc.gov% 2Fcoronavirus% 2F2019-ncov % 2Finfection-control% 2Fcontrol-advice.html (2020).
9. Дхиман, Н. et al. эффективность собранных пациентами мазки на грипп тестирование.майонез Clin. Proc. 87, 548–554 (2012).
10. Ким, Й.-Г. et al. сравнение образцов слюны и мазков из носоглотки для выявления респираторных вирусов с помощью множественной обратной транскрипции-ПЦР. J. Клин. Микробиол. 55, 226–233 (2017).
11. Вилли, А. L. et al. молекулярный надзор за носоглоточным носительством стрептококка pneumoniae у детей, вакцинированных конъюгированными полисахаридными пневмококковыми вакцинами. Наука. Представитель 6, 23809 (2016).
12. К, К. К.-В. et al. последовательное обнаружение 2019 роман Коронавирус в слюне. Клин. Заразить. Дис. (2020) doi: 10.1093 / cid / ciaa149.
13. Кодзима, Н. et al. Самостоятельно собранные мазки из ротовой полости и носа демонстрируют сопоставимую чувствительность с мазками из носоглотки, собранными клиницистом, на наличие Covid-19 Обнаружение. medRxiv 2020.04.11.20062372 (2020).
14. Тран, К., Кимон, К., Северн, М., Пессоа-Сильва, С. L. & Следовательно, J. процедуры образования аэрозолей и риск передачи острых респираторных инфекций медицинским работникам: систематический обзор. плос один 7, e35797 (2012).
15. Джадсон, С. D. & Мюнстер, В. J. нозокомиальная передача новых вирусов через Образующие аэрозоли медицинские Процедуры. вирусы 11, (2019).
16. Ван, Д. et al. клиническая характеристика 138 госпитализированные пациенты С 2019 роман Зараженный коронавирусом пневмония в Ухане, Китай. JAMA (2020) DOI: 10.1001 / jama.2020.1585.
17. Лю, Y. et al. вирусная динамика в легких и тяжелых случаях COVID-19.ланцет Заражение. Дис. (2020) DOI: 10.1016 / S1473-3099 (20) 30232-2.
18. нас. еда & препарат Администрация. ускоренное разрешение на использование в экстренных случаях (EUA) резюме SARS-CoV-2 пробирный (Рутгерс клиническая геномика лаборатория). https: / / www.fda.gov / media / 136875 / скачать.
19. Лауэр, С. А. et al. Инкубационный период Коронавирус болезнь 2019 (COVID-19) От публично сообщается подтверждено Случаи: оценка и применение. Энн. Стажер. Мед.
Источник: https: / / www.medrxiv.org / content / 10.1101 / 2020.04.16.20067835v1.full.pdf
AnneL.Wyllie1 *, JohnFournier2, ArnauCasanovas-Massana1, MelissaCampbell2, MariaTokuyama3, Павитра Vijayakumar4 , Берти Geng4 , М. Екатерина Мюнкер1 , Адам Дж. Moore1 , Шанталь Б.Ф. Vogels1 , Мэри Э. Petrone1 , Изабель М. Ott5, Peiwen Lu3 , Арвинд Venkataraman3 , Алиса Лу-Каллиган3 , Джонатан Klein3 , Ребекка Earnest1 , Михаил Симонов6 , Рупак Datta2 , Райан Handoko2 , Нида Наушад2 , Лоренцо Р. Sewanan2 , Иордания Valdez2 , Элизабет Б. Белый1 , Сара Lapidus1 , Чейни С. Калинич1 , Сяодун Jiang3 , Дэниел Дж. Kim3 , Эрико Kudo3 , Мелисса Linehan3 , Тяньян Mao3 , Мию Морияма3 , Джи Ын Oh3 , Аннси Park3 , Хулио Silva3 , Эрик Song3 , Такехиро Takahashi3 , Манабу Таура3 , Орр-Эль Weizman3 , Патрик Wong3 , Есинь Ян3 , Сантос Bermejo7 , Камила Odio8 , Саад Б. Omer1,2,9,10, charles S. Дела Cruz7 , ShelliFarhadian2, RichardA.Martinello2,7,11, AkikoIwasaki3,12, NathanD.Grubaugh1 # *, AlbertI.Ko1 # *
1 кафедра эпидемиологии микробных заболеваний, йельская школа общественного здравоохранения, нью-хейвен, ct 06510, сша 2 кафедра медицины, секция инфекционных болезней, йельская медицинская школа, нью-хейвен, штат коннектикут, 06510, сша
3 кафедра иммунобиологии йельской медицинской школы, нью-хейвен, штат Коннектикут, 06510, сша
4 отделение акушерства, гинекологии и репродуктивных наук, Йельская школа медицины, Нью-Хейвен, Коннектикут, 06510, США
5 факультет экологии и эволюционной биологии йельского университета, нью-хейвен, ct 06520, сша
6 программа прикладных трансляционных исследований, Йельская школа медицины, Нью-Хейвен, Коннектикут, 06510, США
7 отделение внутренней медицины, отделение легочной медицины, реанимации и медицины сна, Йельская школа медицины, Нью-Хейвен, Коннектикут, 06510, США
8 Медицинский факультет Северо-Восточной Медицинской Группы, Йель-Нью Haven Health, нью-хейвен, ct 06510, сша
9. йельский институт глобального здравоохранения, нью-хейвен, ct 06510, сша
Йельская школа медсестер 10, нью-хейвен, ct 06510, сша
11 отделение профилактики инфекций, Йель-Нью Haven Health, Нью-Хейвен, ct 06520
12.Медицинский институт Говарда Хьюза, нью-хейвен, ct 06510, сша
# соавторы
* Переписка: anne.wyllie@yale.edu (ALW); nathan.grubaugh@yale.edu (NDG); albert.ko@yale.edu (АИК)